糖鎖創薬研究拠点
糖鎖の役割を解明して免疫療法に役立てる
――糖質科学と医学を結びつけ、新たな免疫療法を構築し創薬につなげる
研究キーワード:免疫学、生化学、糖鎖生物学
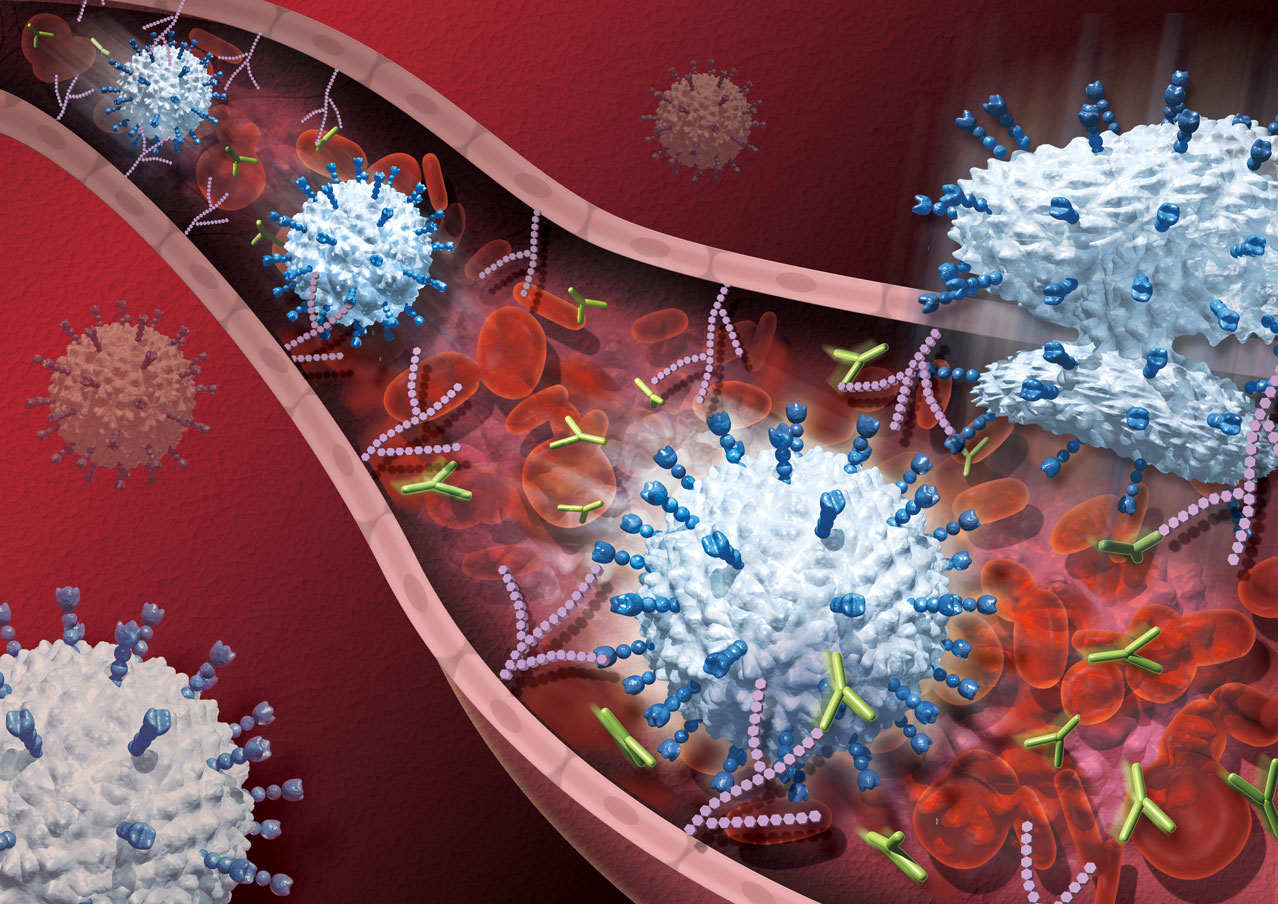 © Akiko Sato
© Akiko Satoリンパ球は、体内の敵と戦う細胞である。
血流に乗って循環し、体内の脾臓やリンパ節などの部位にて活性化を受け、有害な細菌やウイルス、がん細胞などと戦う。糖鎖は、研究者が注目しているリンパ球ホーミングと呼ばれるリンパ球の移動過程に不可欠なものである。研究者は、糖鎖に注目することで、新たな免疫療法や自己免疫疾患の治療薬の発見につながるのではと、期待を高めている。
糖分子が鎖状に結合した糖鎖は、体内で様々な機能を果たしています。リンパ球ホーミングにおいても非常に重要な役割を果たしていることが分かってきました」。薬学研究院免疫微生物学研究室の教授、川島博人はこう話す。
「糖鎖は、リンパ節の内皮細胞の表面に存在しています。糖鎖のおかげで、リンパ球は内皮細胞の表面を認識し、結合することができるのです」 。
リンパ節は、リンパ球が病気と戦うことができるように、リンパ球を活性化させる。 2005年に『ネイチャー・イムノロジー(Nature Immunology)』誌に発表した研究の中で、川島と日米の研究者らは、マウス実験により、二つの酵素(GlcNAc6ST-1とGlcNAc6ST-2)によって 産生される糖鎖が、リンパ球と内皮細胞の結合に不可欠であり、リンパ球ホーミングの制御において非常に重要な役割を果たしていることを明らかにした。
カリフォルニア州にあるサンフォードバーナムプレビス医学研究所(Sanford Burnham Prebys Medical Discovery Institute)でこの研究を行った後、川島は、2005年に帰国し、上記ふたつの 重要酵素を欠損させた「ノックアウト」マウスを日本に持ち帰った。千葉大学では、このマウスを用いて、糖鎖を標的とする新たな抗体を探し続けている。
糖鎖創薬の登場
糖質科学と糖鎖創薬分野の拡大により、種々の疾患における創薬と診断法に飛躍的な進歩がもたらされた。
2017年8月に開設された千葉大学の糖鎖創薬研究拠点は、日本におけるこのような飛躍的 進歩をさらに加速することが期待されている。
「これまで千葉大学の多くの研究者は、それぞれ独立して、糖鎖に関する研究を進めてきました。生物学的機能を専門とする研究者もいれば、糖鎖の構造の合成や分析を重点的に行っている研究者もいます。これら全ての研究者を一カ所に集め、新たな協力関係を構築し、多くの生物学的現象にわたって様々な作用を持つ糖鎖の機能を理解しようとしています」(川島)。この研究拠点は、国内外で協力関係の構築を進めており、国内では産業技術総合研究所(AIST)にある糖鎖創薬技術研究センターのチームと共同研究を進めている。
川島らは、糖鎖のビルディングブロック(構成単位)と特異的に結合し、それらを不活化する抗体を既に複数開発しており、その研究成果を2010年と2015年に『米国生化学・分子生物学会誌(The Journal of Biological Chemistry)』に発表している。これらの抗体により、免疫系が過剰 反応する自己免疫疾患に伴う機能障害を止めることができる可能性がある。
「一般に、糖鎖に対するモノクローナル抗体を開発するのは非常に困難です」と、川島は話す。これらの抗体の開発が難しいのは、一般に糖鎖抗原には免疫原性がほとんどないためである。「その問題を克服するために、私たちは、糖鎖合成酵素ノックアウトマウスを、その欠損酵素を過剰発現する細胞で免疫する方法を用いました」。
次のステップは、創薬のための新たなアイデアを実験的に検証するとともに、製薬会社と協力し、そのアイデアを創薬につなげることである。 「現在、抗体医薬が数多く市販されています」と、川島。これらの抗体医薬は、関節リウマチやがんといった疾病を対象としているが、新たにターゲットにするべき分子が少ないため、この先期待できる進歩は限られている。「その点、糖鎖は、これまで抗体医薬のターゲットとされてこなかったため、未開拓の可能性を秘めています。今こそまさに、糖質科学を利用して新たな候補薬の開発に取り組む、刺激的な時期と言えます」 。
Members
推進責任者
| 研究者名 | 役職名 | 専門分野 |
|---|---|---|
| 川島 博人 | 教授(薬学研究院) 総括 |
免疫学、糖鎖生化学 |
中核推進者(学内研究グループ構成員)
| 研究者名 | 役職名 | 専門分野 |
|---|---|---|
| 伊藤 素行 | 教授(薬学研究院) | 分子生物学、細胞生物学 |
| 土肥 博史 | 教授(園芸学研究院) | 糖化学 |
| 西田 紀貴 | 教授(薬学研究院) | 構造生物学、NMR |
| 山口 憲孝 | 准教授(薬学研究院) | 細胞生物学 |
| 松本 泰典 | 助教(医学部附属病院) | 消化器外科学 |
研究成果報告(2017年〜2019年)
糖鎖は、細胞外の環境の変化や細胞の状態の変化などに応じてダイナミックに構造を変化させることから病態バイオマーカーとして有用であるとともに、抗体医薬等の分子標的薬の創薬標的として有望である。しかし、これまでの分子標的薬の創薬標的としては、主としてタンパク質に焦点が当てられており、糖鎖を標的とした抗体医薬開発の前例はない。この主な理由として、糖鎖研究には一般的に普及している分子生物学的手法のみでは解析できない特殊な分析技術や経験を必要とすること、および特定の糖鎖構造に特異的に結合する抗糖鎖抗体の作製が容易でないことがあげられる。我が国の糖鎖生化学の歴史は古く、その研究は糖鎖構造の精密な解析から生合成経路の解明、生理学的・病理学的機能の解明に至るまで常に世界をリードしてきた。実際に糖鎖の生合成に関与する糖鎖遺伝子の約60%は日本で遺伝子クローニングされ、その機能解析が精力的に進められている。千葉大学には、このような我が国の糖鎖生化学の強みを引き継ぐ研究者が多数所属しており、糖鎖創薬に焦点化して相互連携を図ることにより、千葉大学の強みとなり得る特徴ある研究を先鋭化することができると考えられる。
これまでに推進責任者の川島は、リンパ球の体内動態と獲得免疫応答において、硫酸化された特殊な糖鎖が必須の働きをすることを、独自に開発した糖鎖合成酵素遺伝子欠損マウスを用いて証明してきた(Kawashima et al., Nat. Immunol., 2005)。また、日本医療研究開発機構 (AMED)「糖鎖利用による革新的創薬技術開発事業」の研究代表として、糖鎖合成酵素欠損マウスを同酵素の過剰発現細胞で免疫することにより、体系的かつ高効率に目的とする糖鎖構造を特異的に認識する抗糖鎖モノクローナル抗体を作製できる新しい方法論を開発し、特定の糖鎖に対する親和性および特異性の高い良質な抗体の作製に成功している(Hirakawa et al., J. Biol. Chem., 2010; Matsumura et al., J. Biol. Chem., 2015)。この論文は、”JBC Papers of the Week”に選定され、国際的に高い評価を得ている。
本推進研究では、この方法論を独自の技術シーズとし、革新的な抗糖鎖抗体医薬創成に向けた技術基盤の確立を行うとともに、千葉大学内における糖鎖関連研究者を中心に「糖鎖創薬研究拠点」を形成することにより、千葉大学発の糖鎖創薬に向けた共同研究、技術協力、情報交換を行うための基盤の確立を行った。また、その過程で糖鎖を認識する特異性の高い各種のモノクローナル抗体の樹立に成功するとともに、その医療応用に向けた基礎的な知見を得ることができた。また、糖鎖合成法の開発や糖鎖の生理機能解明等も精力的に推進した。2020年度からは、これまでに培った研究基盤に基づいて、「千葉大学糖鎖創薬研究拠点の創薬シーズ探索への展開」を図ることを計画している。
